Les États-Unis ont reçu un coup de pouce dans leurs efforts pour effectuer davantage de tests COVID-19 après que la Food and Drug Administration (FDA) accordé autorisation d'utilisation d'urgence pour un kit fabriqué par les Laboratoires Abbott.
Le test, appelé BinaxNOW, ne prend que 15 minutes pour produire un résultat et coûte seulement 5 $. Il s’agit d’une procédure de prélèvement nasal effectuée par des professionnels de la santé et d’une petite carte réactive affichant le résultat.
Vidéos recommandées
Abbott dit il prévoit d'expédier des dizaines de millions de kits de test en septembre, pour atteindre 50 millions d'unités par mois début octobre.
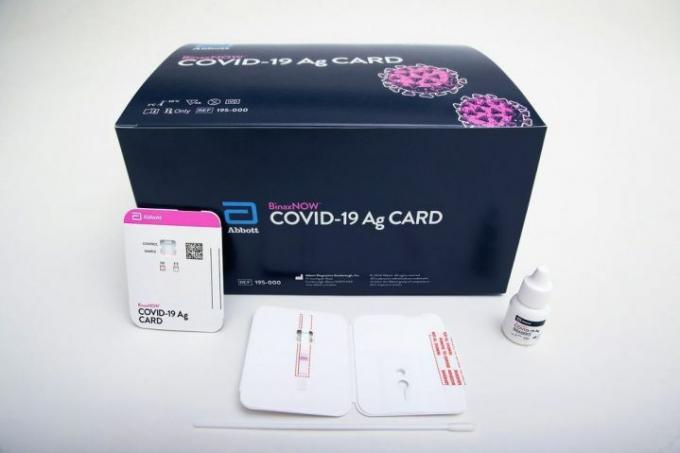
BinaxNOW est un test antigénique, permettant des résultats plus rapides que les tests PCR plus utilisés qui nécessitent un équipement de laboratoire et peuvent prendre des jours, voire des semaines, avant qu'un patient reçoive un résultat.
L'avantage de rapidité apporté par les tests antigéniques peut signifier des résultats moins fiables, mais dans une étude clinique menée par Abbott avec plusieurs leaders américains Dans les universités de recherche, le test BinaxNOW a correctement diagnostiqué les personnes atteintes de la maladie dans 97,1 % des cas, tout en excluant correctement celles qui n'en étaient pas atteintes dans 98,5 % des cas. le temps.
La société basée dans l’Illinois lancera son test avec une application mobile appelée Navica qui peut fonctionner comme un « passe-santé numérique temporaire » pour ceux dont le test est négatif.
« Cette application unique en son genre, disponible gratuitement, permettra aux personnes dont le test est négatif d'afficher un pass sanitaire numérique temporaire qui est renouvelé chaque fois qu'une personne est testée par son fournisseur de soins de santé avec la date du résultat du test », a déclaré Abbott dans un communiqué. "Les organisations pourront visualiser et vérifier les informations sur un appareil mobile pour faciliter l'entrée dans les installations ainsi que le lavage des mains, la distanciation sociale, un nettoyage amélioré et le port d'un masque."
Robert B. Ford, président et chef de la direction d'Abbott, a déclaré: « BinaxNOW et l'application Navica nous offrent une solution abordable et facile à utiliser. test évolutif, et un outil numérique de santé complémentaire pour nous aider à avoir un peu plus de normalité dans notre quotidien vies."
La nouvelle d’Abbott arrive quelques jours seulement après que la FDA a délivré une autorisation d’utilisation d’urgence pour l'utilisation de plasma sanguin de convalescence dans le traitement des patients atteints du COVID-19.
Les États-Unis sont actuellement le pays le plus touché en termes de nombre de décès liés au COVID-19, avec un peu plus de 183 000 au 26 août 2020.
Recommandations des rédacteurs
- Obtenez le rappel du COVID-19, aurait dit Apple au personnel
- Apple Maps vous montre désormais les lieux de vaccination contre le COVID-19
- La meilleure technologie COVID du CES 2021: masques et désinfectants intelligents
- Ce distributeur automatique distribue des tests COVID, pas des barres chocolatées
- Les dernières fonctionnalités de Google Maps visent à réduire le stress des fêtes de fin d'année
Améliorez votre style de vieDigital Trends aide les lecteurs à garder un œil sur le monde en évolution rapide de la technologie avec toutes les dernières nouvelles, des critiques de produits amusantes, des éditoriaux perspicaces et des aperçus uniques.




