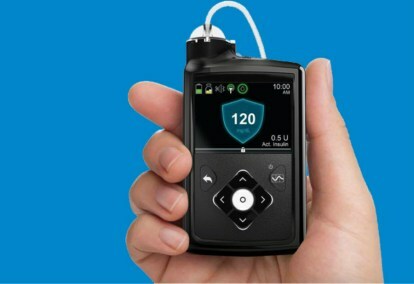
Система Medtronic MiniMed 670G — це переносний пристрій, який поєднує безперервний моніторинг рівня глюкози в крові — визначення рівня цукру в крові — з інсуліновою помпою. Алгоритм, який використовувався для коригування дозування інсуліну під назвою SmartGuard HCL, був останнім кроком у поетапній розробці системи замкнутого циклу Medtronic.
Рекомендовані відео
За словами Річарда М. Бергенстал, доктор медичних наук, головний дослідник дослідження та виконавчий директор Міжнародного центру діабету Парк Ніколлет у Міннеаполісі, «Дані основного дослідження були переконливими, і я впевнений, що ця терапія буде добре сприйнята як клініками, так і пацієнтами спільнота».
JDRF також з ентузіазмом. «Ця важлива віха є важливим кроком уперед у лікуванні діабету 1 типу покращити якість життя тих, хто живе з цією хронічною хворобою», – сказав Дерек Рапп, президент JDRF і генеральний директор. «Нас дуже надихає швидкість, з якою FDA схвалила цю новаторську технологію, і ми пишаємося роллю, яку JDRF зіграв у досягненні цього захоплюючого прориву. Medtronic і JDRF прагнуть забезпечити належний доступ пацієнтів до цієї терапії».
Система MiniMed 670G включає монітор глюкози Guardian Sensor від Medtronic, який має сім днів роботи від батареї. На додаток до контролю рівня глюкози, Guardian також самостійномонітори датчик — якщо пацієнти покладаються на датчик, будь-яка поломка може бути фатальною, тому самодіагностика життєво важлива. Це перший і поки що єдиний датчик, схвалений FDA для систем із замкнутим контуром. Алгоритм SmartGuard HCL має можливість визначати потреби пацієнта в інсуліні, щоб переконатися, що рівень глюкози залишається в межах оптимального цільового діапазону. Єдина дія, яку вимагають пацієнти, це введення споживання вуглеводів під час їжі та періодичне калібрування датчика. Більше ніяких пальців, вимірювань і самостійних ін'єкцій інсуліну.
Комерційний випуск і доступність MiniMed 670G очікується навесні 2017 року, а схвалення регуляторних органів в інших країнах очікується цього літа.
Рекомендації редакції
- FDA дозволило першу в історії програму для смартфонів для доставки інсуліну
Оновіть свій спосіб життяDigital Trends допомагає читачам стежити за динамічним світом технологій завдяки всім останнім новинам, цікавим оглядам продуктів, проникливим редакційним статтям і унікальним у своєму роді коротким оглядам.



