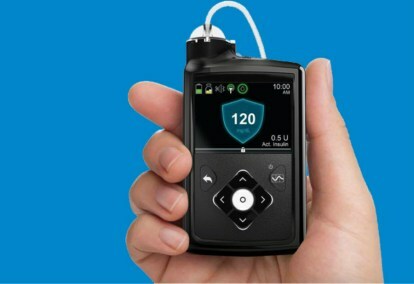
O sistema Medtronic MiniMed 670G é um dispositivo vestível que combina monitoramento contínuo da glicemia – teste de glicemia – com uma bomba de insulina. O algoritmo utilizado para ajustar a dosagem de insulina, denominado SmartGuard HCL, foi o último passo no desenvolvimento faseado do sistema de circuito fechado da Medtronic.
Vídeos recomendados
De acordo com Ricardo M. Bergenstal, MD, investigador principal do estudo e diretor executivo do Park Nicollet International Diabetes Center em Minneapolis, “Os dados do ensaio principal foram convincentes e estou confiante de que esta terapia será bem recebida tanto pelos clínicos como pelos pacientes. comunidade."
O JDRF também está entusiasmado. “Este marco significativo representa um importante passo em frente na gestão da diabetes tipo 1 e irá melhorar a qualidade de vida daqueles que vivem com esta doença crônica”, disse Derek Rapp, presidente da JDRF e CEO. “Estamos muito encorajados pela velocidade com que esta tecnologia inovadora foi aprovada pela FDA e estamos orgulhosos do papel que a JDRF desempenhou na obtenção deste avanço emocionante. A Medtronic e a JDRF estão empenhadas em garantir o acesso adequado dos pacientes a esta terapia.”
O sistema MiniMed 670G inclui o monitor de glicose Guardian Sensor da Medtronic, que tem bateria com duração de sete dias. Além de monitorar os níveis de glicose, o Guardian também auto-monitores o sensor — se os pacientes confiarem no sensor, qualquer avaria poderá ser fatal, por isso o autodiagnóstico é vital. Este é o primeiro e até agora único sensor aprovado pela FDA para sistemas de circuito fechado. O algoritmo SmartGuard HCL tem a capacidade de aprender as necessidades de insulina do paciente para garantir que os níveis de glicose permaneçam dentro da faixa ideal. As únicas ações exigidas pelos pacientes são inserir a ingestão de carboidratos nas refeições e calibrar periodicamente o sensor. Chega de múltiplas punções digitais, medições e injeções de insulina autoadministradas.
O lançamento comercial e a disponibilidade do MiniMed 670G são esperados na primavera de 2017 e a aprovação regulatória em outros países é esperada naquele verão.
Recomendações dos Editores
- FDA libera primeiro aplicativo de smartphone para entrega de insulina
Atualize seu estilo de vidaDigital Trends ajuda os leitores a manter o controle sobre o mundo acelerado da tecnologia com as últimas notícias, análises divertidas de produtos, editoriais criteriosos e prévias únicas.




