על משהו שנקרא "שם מוכר לביולוגים מולקולריים," רבים מכם כנראה מעולם לא שמעו על CRISPR, ואינם יודעים מדוע אתם צריכים להתרגש (או, אולי, לפחד). זה הכל על ריפוי גנטי מתקדם וחבור - וזה מביא רעיונות מדע בדיוני היישר למציאות. הנה שאלות נפוצות קצרות על המדע שמאחורי CRISPR ומדוע העולם שם לב כל כך.
אוקיי, מה זה CRISPR ומה זה מייצג?
CRISPR מתייחס לרצפי DNA יוצאי דופן המסייעים בהגנה על אורגניזמים על ידי זיהוי איומים - במיוחד וירוסים - ותקיפתם. השם מייצג מקובצים ברווחים קבועים קצרים פלינדרום חוזר. כן, זה נשמע קצת מגוחך, אבל זה למעשה תיאור מדויק מאוד כשמסתכלים על רצפי ה-DNA עצמם. הם מקובצים, הם מרווחים במרווחים ברורים, וכאשר מוקצים להם ערכי אותיות הם אכן נראים כמו פלינדרומים קצרים שחוזרים שוב ושוב עם שינויים קלים.
סרטונים מומלצים

CRISPRs הבחינו לראשונה כבר בשנות ה-80, כאשר מדענים חקרו את הגנום של ארכיאה וחיידקים. אפילו בגנומים פשוטים יחסית כל כך, ביולוגים (בעיקר פרנסיסקו מוג'יקה) החלו להבחין ברצפים המוזרים הללו שנראה כי הם חוזרים על עצמם בצורה מאוד ספציפית, עם רווחים ביניהם. ביולוגים מולקולריים היו בטוחים שיש להם מטרה ייחודית, והתיאוריה הרווחת הפכה במהרה להגנה ויראלית, מה שהוכח לבסוף ב-2007 בניצוחו של פיליפ הורבאת. עם זאת, רק בתחילת שנות ה-2010 החלו החוקרים להתלהב במיוחד מהפוטנציאל מאחורי CRISPR.
קָשׁוּר
- עריכת גן CRISPR-Cas9 יכולה יום אחד 'לכבות' את נגיף ה-HIV בגוף
- על פי הדיווחים, רופאים סינים ילדו את התינוקות הראשונים בעולם שעברו עריכת גנים
אז זה רק גדיל DNA?
כן ולא. CRISPR הפך למאפשר של שחבור גנים, עריכה וניסויים כלליים. כדי להבין איך, חשוב להבין תחילה את התפקיד של CRISPRs בגנום, וכיצד הם פועלים כדי להגן על אורגניזמים (בדרך כלל, כפי שציינו, חיידקים). השוואה הוגנת תהיה טלגרפים ששולחים קוד מורס. כל רצף הוא הודעה על התקפה אחרת, וכל רווח הוא ה-STOP שמסיים את ההודעה הזו. אם מטפורות הן לא הקטע שלך, הרווארד נכנס הרבה יותר לעומק.
כאשר אורגניזם נתקל בנגיף חדש ומסוכן, הוא לא יודע איך להגן על עצמו או להביס את הנגיף - הוא צריך ללמוד, בדיוק כפי שעושות רוב התגובות החיסוניות. זה יכול להיות מסובך, כי וירוסים תוקפים DNA ישירות... אבל זה גם הופך אותם לפגיעים בדרכים מסוימות. רצפי ה-CRISPR גונבים גדילי DNA מרכזיים מהנגיף ושומרים אותם בהודעות קוד מורס קטנות. כאשר וירוס דומה תוקף שוב, CRISPR מגיב, "אה, אנחנו מזהים את זה: הנה איך להביס אותו!" וזה שולח את הודעת קוד המורס הרלוונטית לשדה הקרב.
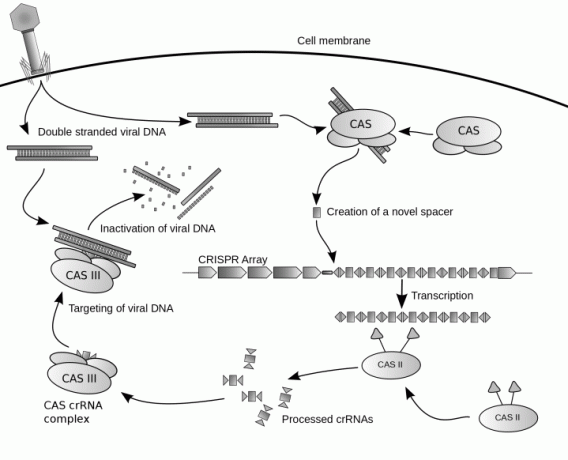
שם, חיילי CRISPR קטנים בשם Cas - אנזימים המיוצרים במיוחד עבור המשימה הזו וממוספרים לפי מטרתם - להיקשר ל-DNA ויראלי ולחתוך אותו בנקודת התורפה שלו, לפי המידע המקודד ב- הוֹדָעָה. זה משבית את הנגיף ומאפשר לאורגניזם להגן על עצמו בהצלחה.

…בסדר. למה זה משנה שוב?
כי - וקשה להמעיט בחשיבות של זה - בעוד CRISPR משתמש רק בטלגרף שלה מערכת הגנה מפני וירוסים, מדענים הבינו שהם יכולים להשתמש בטלגרף הזה לתקשר כל דבר. לסגור גן? בטח (זה אפילו לא חייב להיות גן ויראלי). להפעיל גן? אין בעיה - פשוט בטלגרף את ההוראה הנכונה אל חיילי האנזים Cas. CRISPR-Cas9 בפרט יכול להפוך לכלי מצוין לחיתוך, שילוב מחדש ולעריכת DNA בדרך כלל, כל עוד הוא מקבל את ההודעות הנכונות.
במשך שנים, מדענים עובדים על דרכים לשלוט ב-Cas9, ובהמשך, לפתח מדריכי RNA קטנים עבור ה-Cas9 חיילים ואפילו חיילים משלימים קוראים Cpf1, שהם טובים יותר בהסתננות וחילוץ ללא סיכון מוּטָצִיָה. בהשוואה לזה, הכלים הישנים והמסורבלים של מניפולציה גנטית נראו כמו מועדונים של אנשי מערות לצד לייזרים כירורגיים. זה הפך לחדשות ענק בקהילה המדעית, ולמעשה התחילו כמה קרבות בין קבוצות וחוקרים שונים על מי ראוי לקרדיט על מה.

בינתיים הכל טוב. אבל למה זה עניין גדול בעולם הטכנולוגיה?
מכיוון שאנחנו כרגע בתחילתו של פרץ ענק של ניסויים ב-CRISPR. המכשירים הרפואיים והידע המדעי שלנו הגיעו לנקודה שבה נוכל ליישם את כל מה שלמדנו מ-CRISPR הלכה למעשה ולהתחיל לבצע ניסויים מהירים ויעילים על שחבור גנים. למעוניינים בחוד החנית, עַיִט-מעללי מדע ראויים, זה המקום להיות בו.
בֶּאֱמֶת? אתה אומר שאנחנו יכולים לערוך כֹּל אֶחָדה-DNA של עכשיו?
שאלה טובה. אנחנו עדיין לא שם, אבל נערכו כמה ניסויים מבטיחים. נוצר זוג קופים עם שינויים גנים ספציפיים באמצעות מוטציות ממוקדות באמצעות טכניקות CRISPR. המטרה כאן הייתה לזהות בעיות גנטיות לפני הלידה ולשבש את הגנים הפגומים כך הם לא יכולים לעשות שום נזק (זה היה גם עניין גדול שזה עבד עם קופים במקום רק עם עכברים). ניסויים אחרים הראו שאפשר גם להשתמש בתהליך לשנות את ה-DNA בבטחה כדי להתנגד לזיהום ב-HIV.
עם זאת, הניסוי המרגש ביותר מתקיים בסין, שם מדענים מנסים להשתמש בטכניקות CRISPR כדי להסיר DNA פגום מהתאים של חולי סרטן ריאות חיים ומבוגרים. יש הרבה עיניים על הפרויקט הזה כדי לראות כמה הוא מוצלח.
בסדר: איך נראה העתיד של CRISPR?
יש לנו הרבה עבודה לעשות. ראוי לציין שהניסויים שהוזכרו לעיל דרשו תקופה ארוכה של מחקר יקר והרבה מאוד מקרים כושלים לפני הושגה הצלחה - וגם אז, ללמוד כיצד לחזור על הניסויים הללו במדויק ידרוש עבודה והשקעה רצינית.
אבל זה יותר על עידון מאשר תגליות חדשות: במילים אחרות, זה רק עניין של זמן עד שנלמד להשתמש ב-CRISPR מספיק טוב כדי להביא יישומים לעולם הרפואה. כשזה מתחיל לקרות (וזה יכול להיות רק בעוד מספר שנים), רבות מהשאלות התיאורטיות שיש לנו לגבי מניפולציה של גנים, תינוקות מעצבים, אורגניזמים מנשקים, הגדלה אנושית ומערכות תשלום עבור ריפוי הולכים להפוך להרבה יותר מתאורטי.
המלצות עורכים
- עריכת גנים של CRISPR יכולה לעזור לעצור נגיף עופות נפוץ בדרכו
- סאגת התינוקות של CRISPR נמשכת כאשר סין מאשרת הריון שני שנערך בגנים
- עריכת גנים של CRISPR יוצרת עכברים מוגנים לקוקאין, שמטרתה לפצח חידת התמכרות



