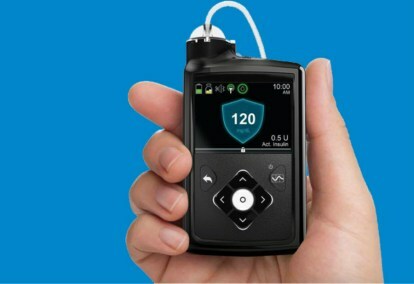
A Medtronic MiniMed 670G rendszer egy hordható eszköz, amely a folyamatos vércukorszint-ellenőrzést – vércukorszint mérést – inzulinpumpával kombinálja. Az inzulinadagolás beállítására használt algoritmus, az úgynevezett SmartGuard HCL, a Medtronic zárt hurkú rendszer fokozatos fejlesztésének utolsó lépése volt.
Ajánlott videók
Richard M. szerint. Bergenstal, M.D., a tanulmány vezető kutatója és a minneapolisi Park Nicollet International Diabetes Center ügyvezető igazgatója, „A kulcsfontosságú vizsgálat adatai meggyőzőek voltak, és biztos vagyok benne, hogy ezt a terápiát a klinikai és a betegek is jól fogadják majd közösség."
A JDRF is lelkes. „Ez a jelentős mérföldkő fontos előrelépést jelent az 1-es típusú cukorbetegség és az akarat kezelésében javítja az ezzel a krónikus betegséggel élők életminőségét” – mondta Derek Rapp, a JDRF elnöke és vezérigazgató. „Nagyon ösztönöz minket az a sebesség, amellyel az FDA jóváhagyta ezt az úttörő technológiát, és büszkék vagyunk a JDRF szerepére ennek az izgalmas áttörésnek az elérésében. A Medtronic és a JDRF elkötelezett amellett, hogy biztosítsák a betegek megfelelő hozzáférését ehhez a terápiához.”
A MiniMed 670G rendszer tartalmazza a Medtronic Guardian Sensor glükózmonitorát, amely hét napos akkumulátor-élettartammal rendelkezik. A glükózszint monitorozása mellett a Guardian önmagát ismonitorok az érzékelő – ha a betegek az érzékelőre támaszkodnak, minden meghibásodás végzetes lehet, ezért az öndiagnosztika létfontosságú. Ez az első és eddig egyetlen érzékelő, amelyet az FDA jóváhagyott zárt hurkú rendszerekhez. A SmartGuard HCL algoritmus képes megtanulni a páciens inzulinszükségletét, hogy megbizonyosodjon arról, hogy a glükózszint az optimális céltartományon belül marad. A betegeknek csak az étkezés közbeni szénhidrátbevitel bevitele és az érzékelő rendszeres kalibrálása szükséges. Nincs több ujjbegyezés, mérés és öninzulin beadás.
A MiniMed 670G kereskedelmi forgalomba hozatala és elérhetősége 2017 tavaszán várható, más országokban pedig nyáron a hatósági jóváhagyás.
Szerkesztői ajánlások
- Az FDA engedélyezte az első okostelefon-alkalmazást az inzulin adagolásához
Frissítse életmódjátA Digital Trends segítségével az olvasók nyomon követhetik a technológia rohanó világát a legfrissebb hírekkel, szórakoztató termékismertetőkkel, éleslátó szerkesztőségekkel és egyedülálló betekintésekkel.

