Za nešto što se zove "poznato ime za molekularne biologe,” mnogi od vas vjerojatno nikada nisu čuli za CRISPR i ne znaju zašto biste trebali biti uzbuđeni (ili, možda, prestravljeni). Sve se vrti oko napredne genske terapije i spajanja - i pretvara znanstveno-fantastične ideje ravno u stvarnost. Evo kratkog FAQ-a o znanosti iza CRISPR-a i zašto svijet obraća tako veliku pozornost.
U redu, što je CRISPR i što znači?
CRISPR se odnosi na neobične sekvence DNK koje pomažu u zaštiti organizama identificiranjem prijetnji – posebno virusa – i njihovim napadom. Naziv stoji za Skupljeni Pravilno razmaknuti Kratki Palindromski Ponavlja se. Da, to zvuči pomalo smiješno, ali zapravo je vrlo točan opis kada se pogledaju same DNK sekvence. Skupljeni su, raspoređeni su u jasnim razmacima, a kada im se dodijele vrijednosti slova, izgledaju poput kratkih palindroma koji se uvijek iznova ponavljaju s malim varijacijama.
Preporučeni videozapisi

CRISPR su prvi put primijećeni davnih 1980-ih kada su znanstvenici proučavali genome arheja i bakterija. Čak iu takvim relativno jednostavnim genomima, biolozi (osobito Francisco Mojica) počeli su primjećivati ove čudne sekvence koje su se ponavljale na vrlo specifičan način, s razmacima između. Molekularni biolozi bili su sigurni da imaju jedinstvenu svrhu, a prevladavajuća teorija ubrzo je postala obrana od virusa, što je konačno dokazano 2007. pod vodstvom Philippea Horvatha. Međutim, tek početkom 2010-ih istraživači su počeli postajati posebno strastveni u pogledu potencijala iza CRISPR-a.
Povezano
- Uređivanje gena CRISPR-Cas9 moglo bi jednog dana 'isključiti' virus HIV-a u tijelu
- Kineski liječnici navodno su rodili prve bebe na svijetu s modificiranim genima
Dakle, to je samo lanac DNK?
Da i ne. CRISPR je postao pokretač spajanja gena, uređivanja i općeg eksperimentiranja. Da bismo razumjeli kako, važno je prvo razumjeti ulogu CRISPR-a u genomima i kako oni djeluju na zaštitu organizama (obično, kao što smo spomenuli, bakterija). Poštena usporedba bila bi telegraf koji šalje Morseov kod. Svaka sekvenca je poruka o drugom napadu, a svaki razmak je STOP koji završava tu poruku. Ako metafore nisu tvoja stvar, Harvard ulazi u mnogo veću dubinu.
Kada se organizam susreće s novim i opasnim virusom, ne zna kako se zaštititi ili pobijediti virus – mora naučiti, baš kao što to radi većina imunoloških odgovora. To može biti nezgodno, jer virusi izravno napadaju DNK...ali to ih također čini ranjivima na određene načine. CRISPR sekvence kradu ključne niti DNK od virusa i čuvaju ih u onim malim Morseovim porukama. Kad sličan virus ponovno napadne, CRISPR odgovara: "Oh, prepoznajemo ovo: Evo kako ga pobijediti!" I šalje relevantnu Morseovu poruku na bojno polje.
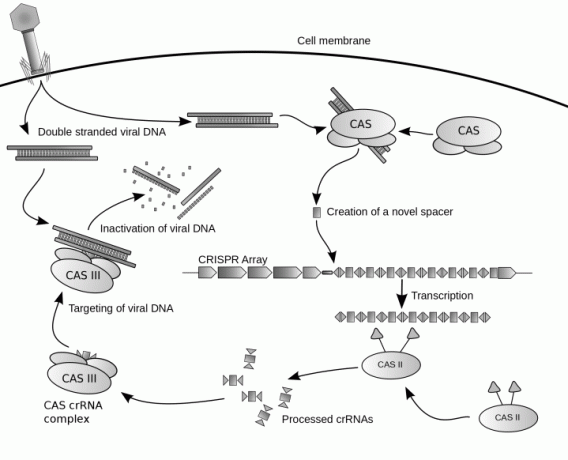
Tamo su mali CRISPR vojnici zvani Cas – enzimi proizvedeni posebno za ovu misiju i numerirani prema njima njihova svrha – vezati se za virusnu DNK i rezati je na njenom slabom mjestu, prema informacijama kodiranim u poruka. Time se virus gasi, a organizmu omogućuje uspješna obrana.

…U redu. Zašto je to opet važno?
Jer – a teško je podcijeniti važnost ovoga – dok CRISPR koristi samo svoj telegraf sustav za obranu od virusa, znanstvenici su shvatili da taj telegraf mogu koristiti za komunicirati bilo što. Ugasiti gen? Naravno (čak i ne mora biti virusni gen). Uključiti gen? Nema problema - samo pošaljite ispravne upute enzimskim Cas vojnicima. Posebno CRISPR-Cas9 može postati izvrstan alat za rezanje, rekombiniranje i općenito uređivanje DNK, sve dok prima prave poruke.
Godinama su znanstvenici radili na načinima kontrole Cas9 i, kasnije, na razvoju malih RNA vodiča za Cas9 vojnici, pa čak i dodatni vojnici koji se nazivaju Cpf1, koji su bolji u infiltraciji i izvlačenju bez rizika od mutacija. U usporedbi s ovim, stari, nezgrapni alati za manipulaciju genima izgledali su poput toljaga pećinskih ljudi pored kirurških lasera. Postala je velika vijest u znanstvenoj zajednici i zapravo je pokrenula nekoliko bitaka između različitih skupina i istraživača oko toga tko je za što zaslužan.

Zasada je dobro. Ali zašto je to velika stvar u svijetu tehnologije?
Zato što smo trenutno na početku velikog naleta CRISPR eksperimenata. Naši medicinski uređaji i znanstveno znanje dosegli su točku u kojoj možemo sve što smo naučili iz CRISPR-a primijeniti u praksi i započeti s brzim, učinkovitim eksperimentima na spajanju gena. Za one koje zanima najnovije, Rese-vrijedan podviga znanosti, ovo je pravo mjesto.
Stvarno? Hoćete reći da možemo uređivati bilo tkoDNK sada?
Dobro pitanje. Još nismo tamo, ali je provedeno nekoliko obećavajućih eksperimenata. Proizveden je par majmuna sa specifičnim promjenama gena kroz ciljane mutacije koristeći CRISPR tehniku. Ovdje je cilj bio identificirati genetske probleme prije rođenja i poremetiti neispravne gene tako da ne mogu učiniti nikakvu štetu (također je bilo važno što je radio s majmunima umjesto samo s miševi). Drugi eksperimenti su pokazali da se proces također može koristiti za sigurno mijenjati DNK kako bi se oduprli HIV infekciji.
Međutim, najuzbudljiviji eksperiment je u tijeku u Kini, gdje znanstvenici pokušavaju koristiti CRISPR tehnike ukloniti oštećenu DNK iz stanica živih, odraslih pacijenata s rakom pluća. Puno je očiju uprto u ovaj projekt kako bi vidjeli koliko je uspješan.
U redu: Kako izgleda budućnost CRISPR-a?
Imamo puno posla. Vrijedno je napomenuti da su gore spomenuti eksperimenti zahtijevali dugo razdoblje skupih istraživanja i mnogo, mnogo neuspješnih slučajeva prije uspjeh je postignut – a čak i tada, učenje kako točno ponoviti te eksperimente zahtijevat će ozbiljan rad i ulaganja.
Ali ovdje se radi više o usavršavanju nego o novim otkrićima: Drugim riječima, samo je pitanje vremena kada ćemo naučiti koristiti CRISPR dovoljno dobro da uvedemo aplikacije u svijet medicine. Kad se to počne događati (a moglo bi biti tek za nekoliko godina), mnoga teorijska pitanja koja imamo o manipulaciji genima, dizajnerske bebe, naoružani organizmi, ljudsko povećanje i sustavi plaćanja za liječenje postat će mnogo više od teorije.
Preporuke urednika
- CRISPR uređivanje gena moglo bi pomoći u zaustavljanju uobičajenog virusa peradi
- Saga o bebi CRISPR nastavlja se dok je Kina potvrdila drugu trudnoću s modificiranim genima
- CRISPR uređivanje gena stvara miševe otporne na kokain, s ciljem rješavanja zagonetke ovisnosti




