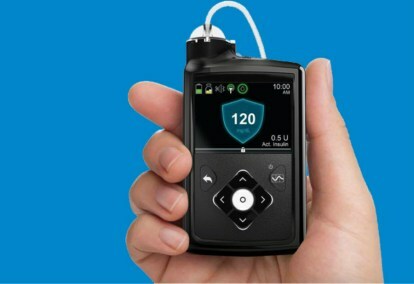
Sustav Medtronic MiniMed 670G nosivi je uređaj koji kombinira kontinuirano praćenje glukoze u krvi — testiranje šećera u krvi — s inzulinskom pumpom. Algoritam korišten za podešavanje doziranja inzulina, nazvan SmartGuard HCL, bio je posljednji korak u Medtronicovom postupnom razvoju sustava zatvorene petlje.
Preporučeni videozapisi
Prema Richardu M. Bergenstal, M.D., glavni istraživač studije i izvršni direktor Park Nicollet International Diabetes Center u Minneapolisu, "Podaci iz ključnog ispitivanja bili su uvjerljivi i uvjeren sam da će ovu terapiju dobro prihvatiti i klinički i pacijenti zajednica."
JDRF je također entuzijastičan. “Ova značajna prekretnica predstavlja važan korak naprijed u upravljanju dijabetesom tipa 1 i bit će poboljšati kvalitetu života za one koji žive s ovom kroničnom bolešću,” rekao je Derek Rapp, predsjednik JDRF-a i DIREKTOR TVRTKE. “Vrlo smo ohrabreni brzinom kojom je ovu revolucionarnu tehnologiju odobrila FDA i ponosni smo na ulogu koju je JDRF imao u postizanju ovog uzbudljivog otkrića. Medtronic i JDRF predani su osiguravanju odgovarajućeg pristupa pacijenata ovoj terapiji.”
Sustav MiniMed 670G uključuje Medtronic Guardian Sensor monitor glukoze, koji ima bateriju koja traje sedam dana. Uz praćenje razine glukoze, Guardian također samostalno kontroliramonitori senzor — ako se pacijenti oslanjaju na senzor, svaki kvar može biti koban, stoga je samodijagnostika vitalna. Ovo je prvi i za sada jedini senzor odobren od strane FDA za zatvorene sustave. Algoritam SmartGuard HCL ima sposobnost saznati koliko je inzulin potreban pacijentu kako bi razine glukoze ostale unutar optimalnog ciljnog raspona. Jedina radnja koju pacijenti zahtijevaju je unos unosa ugljikohidrata tijekom obroka i povremeno kalibriranje senzora. Nema više višestrukih uboda prstima, mjerenja i inzulina koji si sami dajete.
Komercijalno izdanje i dostupnost MiniMed 670G očekuju se u proljeće 2017., a regulatorno odobrenje u drugim zemljama očekuje se tog ljeta.
Preporuke urednika
- FDA odobrila prvu aplikaciju za pametne telefone za isporuku inzulina
Nadogradite svoj životni stilDigitalni trendovi pomažu čitateljima da prate brzi svijet tehnologije sa svim najnovijim vijestima, zabavnim recenzijama proizvoda, pronicljivim uvodnicima i jedinstvenim brzim pregledima.




