Estados Unidos ha recibido un impulso en sus esfuerzos por realizar más pruebas de COVID-19 después de que la Administración de Alimentos y Medicamentos (FDA) otorgada autorización de uso de emergencia para un kit fabricado por Abbott Laboratories.
La prueba, llamada BinaxNOW, tarda sólo 15 minutos en producir un resultado y tiene un precio de sólo 5 dólares. Se trata de un procedimiento de hisopado nasal realizado por profesionales de la salud y una pequeña tarjeta reactiva que muestra el resultado.
Vídeos recomendados
Abbott dicho planea enviar decenas de millones de kits de prueba en septiembre, aumentando hasta 50 millones de unidades por mes a principios de octubre.
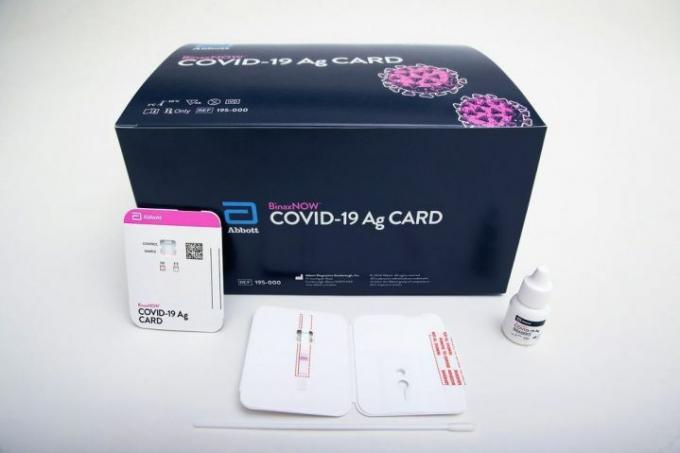
BinaxNOW es una prueba de antígenos que permite resultados más rápidos que las pruebas de PCR más utilizadas, que requieren equipo de laboratorio y pueden tardar días o incluso semanas antes de que un paciente reciba un resultado.
La ventaja de velocidad que conllevan las pruebas de antígenos puede significar resultados menos confiables, pero en un estudio clínico realizado por Abbott con varias empresas líderes de EE. UU. universidades de investigación, la prueba BinaxNOW diagnosticó correctamente a aquellos con la enfermedad el 97,1% de las veces, mientras que descartó correctamente a los que no la padecían el 98,5% de las veces. el tiempo.
La empresa con sede en Illinois lanzará su prueba con una aplicación móvil llamada Navica que puede funcionar como un “pase de salud digital temporal” para quienes den negativo.
“Esta aplicación, primera en su tipo, disponible sin costo alguno, permitirá a las personas con resultados negativos mostrar un pase de salud digital temporal que es Se renueva cada vez que una persona se hace la prueba a través de su proveedor de atención médica junto con la fecha del resultado de la prueba”, dijo Abbott en un comunicado. "Las organizaciones podrán ver y verificar la información en un dispositivo móvil para facilitar el ingreso a las instalaciones junto con el lavado de manos, el distanciamiento social, la limpieza mejorada y el uso de mascarillas".
Roberto B. Ford, presidente y director ejecutivo de Abbott, dijo: "BinaxNOW y la aplicación Navica nos brindan una solución asequible, fácil de usar y prueba escalable y una herramienta de salud digital complementaria para ayudarnos a tener un poco más de normalidad en nuestro día a día. vidas."
La noticia de Abbott llega pocos días después de que la FDA emitiera la autorización de uso de emergencia. para el uso de plasma sanguíneo de convalecientes en el tratamiento de pacientes con COVID-19.
Estados Unidos es actualmente el país más afectado en términos de número de muertes relacionadas con el COVID-19, con un recuento de poco más de 183.000 al 26 de agosto de 2020.
Recomendaciones de los editores
- Reciba la vacuna de refuerzo COVID-19, según se informa Apple le dice al personal
- Apple Maps ahora te muestra los lugares de vacunación COVID-19
- La mejor tecnología COVID de CES 2021: mascarillas y desinfectantes inteligentes
- Esta máquina expendedora ofrece pruebas de COVID, no barras de chocolate
- Las últimas funciones de Google Maps tienen como objetivo aliviar el estrés de la temporada navideña
Mejora tu estilo de vidaDigital Trends ayuda a los lectores a mantenerse al tanto del vertiginoso mundo de la tecnología con las últimas noticias, reseñas divertidas de productos, editoriales interesantes y adelantos únicos.

