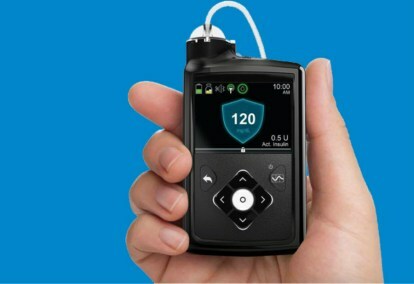
El sistema Medtronic MiniMed 670G es un dispositivo portátil que combina la monitorización continua de la glucosa en sangre (pruebas de azúcar en la sangre) con una bomba de insulina. El algoritmo utilizado para ajustar la dosis de insulina, llamado SmartGuard HCL, fue el último paso en el desarrollo gradual del sistema de circuito cerrado de Medtronic.
Vídeos recomendados
Según Ricardo M. Bergenstal, M.D., investigador principal del estudio y director ejecutivo del Centro Internacional de Diabetes Park Nicollet en Minneapolis, “Los datos del ensayo fundamental fueron convincentes y confío en que esta terapia será bien recibida tanto por el clínico como por el paciente. comunidad."
La JDRF también está entusiasmada. "Este importante hito representa un importante paso adelante en el tratamiento de la diabetes tipo 1 y permitirá mejorar la calidad de vida de quienes viven con esta enfermedad crónica”, dijo Derek Rapp, presidente de JDRF y CEO. “Estamos muy alentados por la velocidad con la que la FDA aprobó esta tecnología innovadora y estamos orgullosos del papel que desempeñó JDRF en el logro de este avance emocionante. Medtronic y JDRF se comprometen a garantizar el acceso adecuado de los pacientes a esta terapia”.
El sistema MiniMed 670G incluye el monitor de glucosa Guardian Sensor de Medtronic, que tiene una duración de batería de siete días. Además de controlar los niveles de glucosa, The Guardian tambiénmonitores el sensor: si los pacientes confían en el sensor, cualquier avería podría ser fatal, por lo que el autodiagnóstico es vital. Este es el primer y hasta ahora único sensor aprobado por la FDA para sistemas de circuito cerrado. El algoritmo SmartGuard HCL tiene la capacidad de conocer las necesidades de insulina del paciente para garantizar que los niveles de glucosa se mantengan dentro del rango objetivo óptimo. Las únicas acciones que deben realizar los pacientes son introducir la ingesta de carbohidratos a la hora de las comidas y calibrar periódicamente el sensor. No más punciones en los dedos, mediciones e inyecciones de insulina autoadministradas.
Se espera el lanzamiento comercial y la disponibilidad del MiniMed 670G en la primavera de 2017 y la aprobación regulatoria en otros países ese verano.
Recomendaciones de los editores
- La FDA aprueba la primera aplicación para teléfonos inteligentes para administrar insulina
Mejora tu estilo de vidaDigital Trends ayuda a los lectores a mantenerse al tanto del vertiginoso mundo de la tecnología con las últimas noticias, reseñas divertidas de productos, editoriales interesantes y adelantos únicos.



