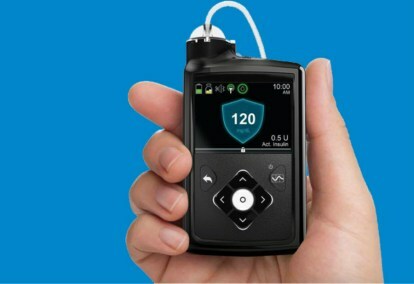
Το σύστημα Medtronic MiniMed 670G είναι μια φορητή συσκευή που συνδυάζει τη συνεχή παρακολούθηση της γλυκόζης του αίματος — μέτρηση σακχάρου στο αίμα — με μια αντλία ινσουλίνης. Ο αλγόριθμος που χρησιμοποιήθηκε για την προσαρμογή της δοσολογίας της ινσουλίνης, που ονομάζεται SmartGuard HCL, ήταν το τελευταίο βήμα στη σταδιακή ανάπτυξη του συστήματος κλειστού βρόχου της Medtronic.
Προτεινόμενα βίντεο
Σύμφωνα με τον Richard M. Bergenstal, M.D., κύριος ερευνητής της μελέτης και εκτελεστικός διευθυντής του Διεθνούς Κέντρου Διαβήτη Park Nicollet στη Μινεάπολη, «Τα δεδομένα από τη βασική δοκιμή ήταν επιτακτικά και είμαι βέβαιος ότι αυτή η θεραπεία θα γίνει καλά αποδεκτή τόσο από τον κλινικό όσο και από τον ασθενή κοινότητα."
Το JDRF είναι επίσης ενθουσιώδες. «Αυτό το σημαντικό ορόσημο αντιπροσωπεύει ένα σημαντικό βήμα προς τα εμπρός στη διαχείριση του διαβήτη τύπου 1 και τη θέληση βελτιώσει την ποιότητα ζωής για όσους ζουν με αυτή τη χρόνια ασθένεια», δήλωσε ο Derek Rapp, πρόεδρος του JDRF και Διευθύνων Σύμβουλος. «Είμαστε πολύ ενθαρρυμένοι από την ταχύτητα με την οποία εγκρίθηκε αυτή η πρωτοποριακή τεχνολογία από τον FDA και είμαστε περήφανοι για τον ρόλο που έπαιξε το JDRF στην επίτευξη αυτής της συναρπαστικής ανακάλυψης. Η Medtronic και η JDRF δεσμεύονται να εξασφαλίσουν την κατάλληλη πρόσβαση των ασθενών σε αυτή τη θεραπεία.»
Το σύστημα MiniMed 670G περιλαμβάνει την οθόνη Guardian Sensor γλυκόζης της Medtronic, η οποία έχει διάρκεια ζωής μπαταρίας επτά ημερών. Εκτός από την παρακολούθηση των επιπέδων γλυκόζης, ο Guardian επίσηςοθόνες ο αισθητήρας — εάν οι ασθενείς βασίζονται στον αισθητήρα, οποιαδήποτε βλάβη μπορεί να είναι θανατηφόρα, επομένως η αυτοδιάγνωση είναι ζωτικής σημασίας. Αυτός είναι ο πρώτος και μέχρι στιγμής μοναδικός αισθητήρας που έχει εγκριθεί από το FDA για συστήματα κλειστού βρόχου. Ο αλγόριθμος SmartGuard HCL έχει τη δυνατότητα να μάθει τις ανάγκες της ινσουλίνης του ασθενούς για να βεβαιωθεί ότι τα επίπεδα γλυκόζης παραμένουν εντός του βέλτιστου εύρους στόχου. Οι μόνες ενέργειες που απαιτούνται από τους ασθενείς είναι να εισάγουν την πρόσληψη υδατανθράκων κατά το γεύμα και να βαθμονομούν περιοδικά τον αισθητήρα. Τέρμα τα πολλαπλά δάχτυλα, οι μετρήσεις και οι αυτοχορηγούμενες βολές ινσουλίνης.
Η εμπορική κυκλοφορία και η διαθεσιμότητα του MiniMed 670G αναμένεται την άνοιξη του 2017 και η ρυθμιστική έγκριση σε άλλες χώρες αναμένεται το καλοκαίρι.
Συστάσεις των συντακτών
- Ο FDA εκκαθαρίζει την πρώτη εφαρμογή smartphone για παροχή ινσουλίνης
Αναβαθμίστε τον τρόπο ζωής σαςΤο Digital Trends βοηθά τους αναγνώστες να παρακολουθούν τον γρήγορο κόσμο της τεχνολογίας με όλα τα τελευταία νέα, διασκεδαστικές κριτικές προϊόντων, διορατικά editorial και μοναδικές κρυφές ματιές.

